*Keskivaikean tai vaikean keuhkoahtaumataudin ylläpitohoito aikuispotilailla, joiden tilaa ei pystytä riittävästi hoitamaan inhaloitavan kortikosteroidin ja pitkävaikutteisen beeta-2-agonistin yhdistelmällä tai pitkävaikutteisen beeta-2-agonistin ja pitkävaikutteisen muskariiniantagonistin yhdistelmällä.
†Astman ylläpitohoito aikuisilla, joilla ei saavuteta riittävää sairauden hallintaa ylläpitohoidolla, joka muodostuu pitkävaikutteisen beeta-2-agonistin ja keskiannoksisen inhaloidun kortikosteroidin yhdistelmästä, ja joilla on ollut vähintään yksi astman pahenemisvaihe kuluneen vuoden aikana.
‡Astman ylläpitohoito aikuisilla, joilla ei saavuteta riittävää sairauden hallintaa ylläpitohoidolla, joka muodostuu pitkävaikutteisen beeta-2-agonistin ja suuriannoksisen inhaloidun kortikosteroidin yhdistelmästä, ja joilla on ollut vähintään yksi astman pahenemisvaihe kuluneen vuoden aikana.
Viitteet:
1. Trimbow inhalaatiosumute valmisteyhteenveto, pharmacafennica.fi
2. Braido, et al. Asthma Research and Practice 2016;2:12
3. Vestbo, et al. Lancet 2017 May 13;389(10082):1919–29
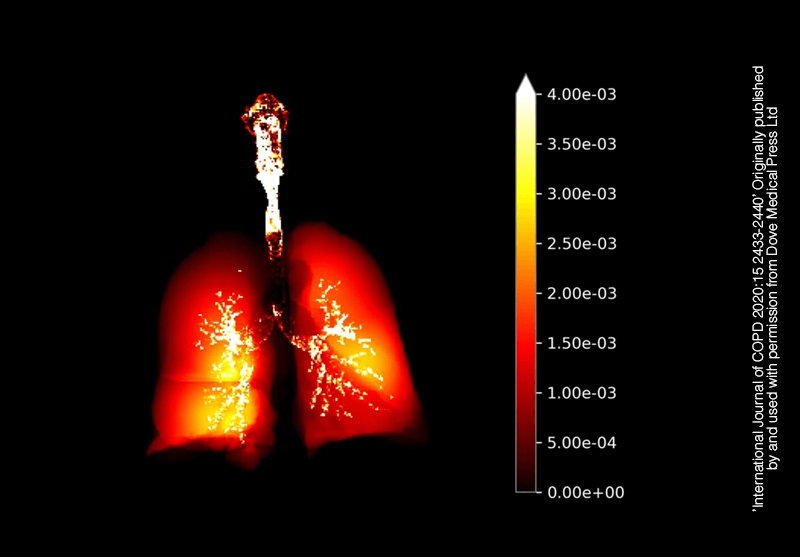
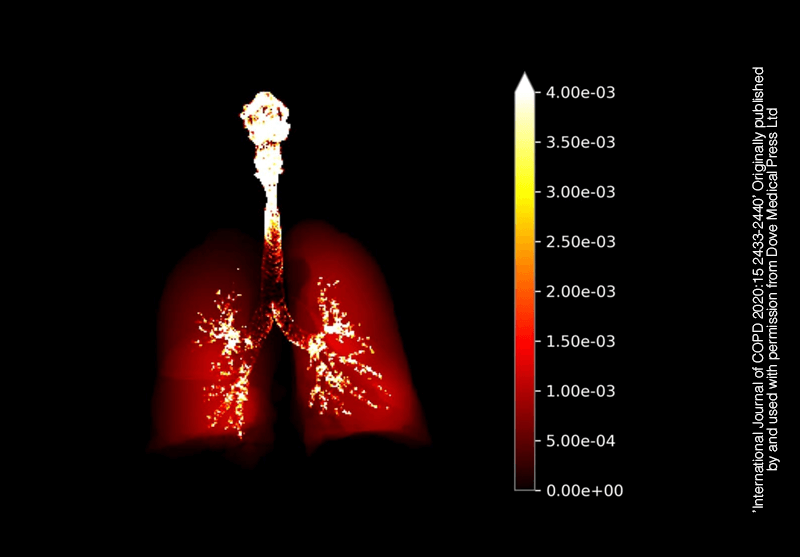
4. Usmani OS, et al. International Journal of COPD 2020;15:2433–40
5. De Backer W, et al. J Aerosol Med Pulm Drug Deliv 2010;23(3):137–48
6. Leach CL, et al. Ann Allergy Asthma Immunol 2012;108(3):195–200
7. Lipworth B, et al. Lancet Respir Med 2014;2:497–506
8. Braido F, et al. World Allergy Organ J 2016;9:37
9. Usmani OS, et al. J Aerosol Med Pulm Drug Deliv 2022;35(4):179–85
10. GOLD Report 2022. Global Strategy for the diagnosis, management, and prevention of COPD. https://goldcopd.org/
11. Trimbow inhalaatiojauhe valmisteyhteenveto, pharmacafennica.fi
Trimbow (beklometasonidipropionaatti, formoterolifumaraattidihydraatti, glykopyrronium) inhalaatiojauhe
Trimbow 88 mikrogrammaa/5 mikrogrammaa/9 mikrogrammaa inhalaatiojauhe
Trimbow 87 mikrogrammaa/5 mikrogrammaa/9 mikrogrammaa inhalaatiosumute, liuos
Trimbow 172 mikrogrammaa/5 mikrogrammaa/9 mikrogrammaa inhalaatiosumute, liuos
Käyttöaihe: Inhalaatiojauhe ja Trimbow 87/5/9 inhalaatiosumute: Keskivaikean tai vaikean keuhkoahtaumataudin (COPD) ylläpitohoito aikuispotilailla, joiden tilaa ei pystytä riittävästi hoitamaan inhaloitavan kortikosteroidin ja pitkävaikutteisen beeta2-agonistin yhdistelmällä tai pitkävaikutteisen beeta2-agonistin ja pitkävaikutteisen muskariiniantagonistin yhdistelmällä. Trimbow 87/5/9 inhalaatiosumute: Astman ylläpitohoito aikuisilla, joiden tila ei pysy riittävästi hallinnassa ylläpitohoitoon käytettävän pitkävaikutteisen beeta2-agonistin ja keskisuuriannoksisen inhaloitavan kortikosteroidin yhdistelmällä, ja joilla on ollut edellisen vuoden aikana vähintään yksi astman pahenemisvaihe. Trimbow 172/5/9 inhalaatiosumute: Astman ylläpitohoito aikuisilla, joiden tila ei pysy riittävästi hallinnassa ylläpitohoitoon käytettävän pitkävaikutteisen beeta2-agonistin ja suuriannoksinen inhaloitavan kortikosteroidin yhdistelmällä, ja joilla on ollut edellisen vuoden aikana vähintään yksi astman pahenemisvaihe. Annostus ja antotapa: Suositeltu annos 2 inhalaatiota kahdesti vuorokaudessa. Enimmäisannos 2 inhalaatiota kahdesti vuorokaudessa. Inhalaatioon. Lääkärin on arvioitava potilaan tilaa säännöllisesti, jotta annokset pysyvät optimaalisina. Astma: Aloitusannosta valittaessa on huomioitava potilaan sairauden vaikeusaste, aiempi astmalääkitys sekä potilaan nykyisten astmaoireiden hallittavuus ja oireiden pahenemisen riski tulevaisuudessa. Lääkärin on arvioitava potilaan tilaa säännöllisesti, jotta annokset pysyvät optimaalisina. Annoksia on pienennettävä pienimpiin annoksiin, joilla astmaoireet pysyvät hyvin hallinnassa. Erityisryhmät: Vaikea maksan vajaatoiminta, vaikea munuaisten vajaatoiminta, dialyysiä edellyttävä loppuvaiheen munuaistauti: valmistetta saa käyttää vain, jos odotettu hyöty on suurempi kuin mahdollinen riski. Pediatriset potilaat: (Keuhkoahtauma: Käyttö ei ole asianmukaista. Astma: Turvallisuutta ja tehoa astman hoidossa ei ole vielä varmistettu.) Potilaalle on näytettävä, miten inhalaattoria käytetään oikein, kehotettava lukemaan pakkausseloste huolellisesti ja noudattamaan ohjeita. Inhalaatiotekniikka on lisäksi syytä tarkistaa ajoittain. Katso lisätiedot valmisteyhteenvedosta. Vasta-aiheet: Yliherkkyys vaikuttaville aineille tai apuaineille. Varoitukset ja käyttöön liittyvät varotoimet: Ei akuuttiin käyttöön. Välittömiä yliherkkyysreaktioita on raportoitu. Paradoksaalista bronkospasmia saattaa esiintyä. Hoitoa ei ole suositeltavaa lopettaa äkillisesti. Kohtauslääkkeiden lisääntynyt käyttö on merkki hoidon uudelleenarvioinnin tarpeesta. Vaikutukset sydämeen ja verisuonistoon: Trimbow-valmistetta on käytettävä varoen, jos potilaalla on sydämen rytmihäiriöitä, etenkin kolmannen asteen eteis-kammiokatkos ja takyarytmiaa, eteisvärinä, idiopaattinen subvalvulaarinen aortan ahtauma, hypertrofinen obstruktiivinen kardiomyopatia, vaikea sydäntauti (etenkin akuutti sydäninfarkti, iskeeminen sydänsairaus, kongestiivinen sydämen vajaatoiminta), ahtauttava verisuonitauti, verenpainetauti ja aneurysma. Hoidossa on oltava varovainen myös, jos potilaalla tiedetään tai epäillään olevan joko synnynnäistä tai lääkehoidosta johtuvaa QT-ajan pitenemistä. Tyreotoksikoosi, diabetes mellitus, feokromosytooma, hoitamaton hypokalemia, ahdaskulmaglaukooma, eturauhasen liikakasvu tai virtsaumpi: varovaisuus tarpeen. Keuhkoahtaumatautipotilaiden tilaa on seurattava keuhkokuumeen mahdollisen kehittymisen varalta. Inhaloitavien kortikosteroidien yhteydessä voi esiintyä systeemisiä vaikutuksia. Aktiivinen tai piilevä keuhkotuberkuloosi tai hengitysteiden sieni- tai virusinfektio: varovaisuus tarpeen. Beeta2-agonistihoito voi johtaa potentiaalisesti vakavaan hypokalemiaan. Varovaisuutta on noudatettava, kun käytössä on useita keuhkoputkia avaavia kohtauslääkkeitä. On suositeltavaa, että seerumin kaliumpitoisuutta seurataan näissä tilanteissa. Veren glukoosiarvoja on tarkkailtava hoidon aikana. Potilaita on neuvottava ottamaan välittömästi yhteyttä lääkäriin, jos heille kehittyy äkillisen ahdaskulmaglaukooman merkkejä tai oireita. Pitkäaikaista antoa yhdessä muiden antikolinergejä sisältävien lääkevalmisteiden kanssa ei suositella. Inhalaation jälkeen suu on huuhdeltava tai kurlattava vedellä nielemättä sitä tai on harjattava hampaat. Jos ilmenee näön hämärtymistä tai muita näköhäiriöitä, potilas on ohjattava silmälääkärille. Inhalaatiojauhe sisältää laktoosia. Inhalaatiosumutteet sisältävät etanolia. Yhteisvaikutukset: Yhteisvaikutus voi olla mahdollinen, jos potilas käyttää myös munuaiseritykseen vaikuttavia lääkevalmisteita. Varovaisuus ja asianmukainen seuranta on suositeltavaa samanaikaisessa käytössä voimakkaiden CYP3A:n estäjien kanssa. Potilaiden on vältettävä ei-kardioselektiivisten beetasalpaajien käyttöä (myös silmätippoina). Hoidossa on oltava varovainen, jos samanaikaisesti määrätään muita beeta-adrenergisiä lääkevalmisteita. Kinidiini, disopyramidi, prokaiiniamidi, antihistamiinit, MAO:n estäjät, trisykliset masennuslääkkeet, fentiatsiinit: samanaikainen käyttö voi pidentää QT-aikaa ja lisätä kammioperäisten rytmihäiriöiden vaaraa. Levodopa, levotyroksiini, oksitosiini ja alkoholi voivat heikentää sydämen beeta2-sympatomimeettien sietoa. MAO:n estäjien ja niiden kaltaisten valmisteiden (esim. furatsolidoni, prokarbatsiini) samanaikainen käyttö voi edistää hypertensiivisten reaktioiden ilmaantumista. Ksantiinijohdannaiset, steroidit, diureetit: beeta2-agonistien mahdolliset hypokaleemiset vaikutukset voivat voimistua. Hedelmällisyys, raskaus ja imetys: Varotoimenpiteenä on suotavaa välttää Trimbow‑valmisteen käyttöä raskauden ja synnytyksen aikana. Käytetään vain jos hyöty potilaalle on suurempi kuin todennäköinen riski sikiölle. Jos imeväisen tai vastasyntyneen äiti on saanut huomattavia määriä Trimbow-valmistetta, lasta on tarkkailtava lisämunuaisten toiminnan lamaantumisen varalta. On päätettävä, lopetetaanko rintaruokinta vai Trimbow-hoito ottaen huomioon rintaruokinnan hyödyt lapselle ja hoidon hyödyt äidille. Eläimillä tehdyissä tutkimuksissa on havaittu hedelmällisyyden heikkenemistä. Haittavaikutukset: Yleiset: Keuhkokuume (keuhkoahtaumatautipotilailla), nielutulehdus, suun kandidiaasi, päänsärky, dysfonia, virtsatieinfektio, nasofaryngiitti. Muut haittavaikutukset, ks. valmisteyhteenveto. Astmapotilailla haittavaikutukset tyypillisesti kertyvät ensimmäisten 3 kk ajalla hoidon aloittamisen jälkeen ja vähenevät pitkäaikaisen käytön myötä (6 kk hoidon aloittamisen jälkeen). Pakkaukset ja hinnat (04-2022): Inhalaatiojauhe 87/5/9: 120 annosta 82,47 €, 3 x 120 annosta 223,78 €. Inhalaatiosumute 87/5/9: 120 annosta 82,47 €, 3 x 120 annosta 223,78 €. Inhalaatiosumute 172/5/9: 120 annosta 82,47 €, 3 x 120 annosta 223,78 € Korvattavuus: Erityiskorvattava reseptilääke. Korvattavuus: Erityiskorvattava reseptilääke. Lisätiedot: Pharmaca Fennica tai Chiesi Pharma AB, Klara Norra Kyrkogata 34, Tukholma, Ruotsi. Tutustu valmisteyhteenvetoon ennen lääkkeen määräämistä. Perustuu 24.3.2022 päivättyyn valmisteyhteenvetoon.